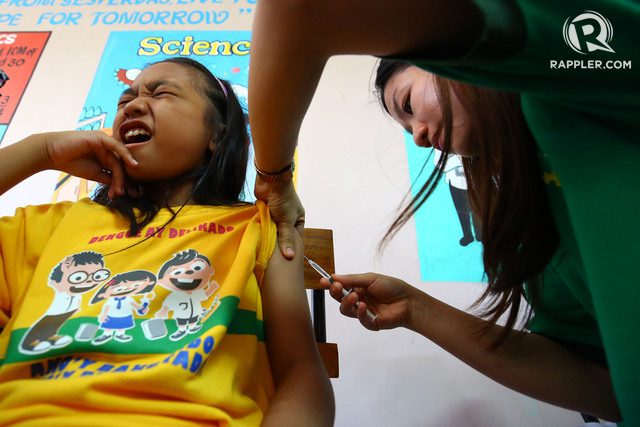
‘Mengapa Dengvaxia mendapatkan persetujuan FDA tanpa izin dari UE?’
keren989
- 0
Ini adalah ringkasan yang dibuat oleh AI, yang mungkin memiliki kesalahan. Untuk konteksnya, selalu rujuk artikel selengkapnya.
Seorang dokter yang menjadi anggota parlemen mempertanyakan mengapa vaksin yang kini menjadi kontroversi mendapat lampu hijau di Filipina
MANILA, Filipina – Jika tidak ditebangi di negara asalnya, mengapa di Filipina?
Seorang dokter yang juga anggota DPR pada Senin, 5 Februari, mempertanyakan Badan Pengawas Obat dan Makanan (FDA) Filipina yang mengizinkan pendaftaran vaksin anti demam berdarah Dengvaxia yang kini kontroversial padahal tidak ada di negaranya. asal, Perancis.
Perwakilan Distrik ke-4 Iloilo Ferjenel Biron, yang juga seorang dokter, mempertanyakan mengapa FDA mengizinkan pendaftaran vaksin ketika masih ditinjau oleh European Medicines Agency (EMA), sebuah lembaga Uni Eropa yang bertanggung jawab mengevaluasi produk medis, harus diselidiki. .
Biron, yang mencatat bahwa dia termasuk di antara mereka yang merancang undang-undang tahun 2009 yang membentuk FDA, menyatakan bahwa “tidak ada produk yang diizinkan untuk diekspor di Filipina jika tidak terdaftar di negara asalnya.”
Melody Samudio dari FDA menjawab bahwa jika suatu produk tidak terdaftar di negara asalnya, badan tersebut kemudian mencari bukti bahwa produk tersebut untuk diekspor, selain persyaratan lainnya.
Ia mencatat bahwa “ada banyak obat-obatan”—bukan hanya Dengvaxia—yang tidak terdaftar di negara asalnya namun telah disetujui untuk didistribusikan di Filipina. Samudio mencatat, hal ini diperbolehkan asalkan memenuhi persyaratan lain, termasuk pemeriksaan kualitas dan efisiensi.
Thomas Triomphe, Kepala Sanofi Pasteur Asia Pasifik, mengatakan vaksin tersebut sudah dalam proses registrasi sebelum EMA. Dia mencatat bahwa perusahaan farmasi Perancis telah mengajukan Dengvaxia untuk ditinjau sehubungan dengan lembaga obat di beberapa negara dan setiap negara memiliki proses evaluasi dan standarnya sendiri.
Biron yang juga ditanyai oleh Sanofi memproduksi botol Dengvaxia bahkan sebelum diberi nomor registrasi di Filipina. Triomphe sendiri membenarkan bahwa produknya telah dikemas ulang untuk didistribusikan di Filipina.
Sekali lagi mengutip aturan FDA, Biron mengatakan registrasi harus dilakukan sebelum produksi.
Mantan kepala FDA Lulu Santiago mengatakan bahwa menurut norma-norma Asia Tenggara, produsen harus memproduksi setidaknya 3 batch, termasuk satu “volume komersial”, sebelum registrasi produk.
Santiago mencatat bahwa “tidak ada batasan” bagi perusahaan yang kemudian menjual batch berukuran komersial yang digunakan untuk validasi “selama memenuhi persyaratan keamanan, kualitas dan kemanjuran.”
Pengadaan vaksin demam berdarah, yang berjumlah lebih dari P3,5 miliar, menjadi subyek penyelidikan di kedua majelis Kongres. Program imunisasi massal, yang dilaksanakan di bawah pemerintahan Aquino, sebelumnya kontroversial, di tengah klaim beberapa ahli medis bahwa uji klinis lebih lanjut harus dilakukan sebelum diperkenalkan ke publik.
Pada akhir November 2017, Sanofi mengakui bahwa data klinis baru menunjukkan bahwa vaksin tersebut menimbulkan risiko lebih besar bagi orang-orang yang belum tertular virus sebelum imunisasi. Data tersebut merupakan hasil data klinis selama 6 tahun.
Filipina, di bawah pemerintahan Duterte, kini meminta pengembalian dana penuh sebesar P3,5 miliar dari Sanofi.
Panel dari Rumah Sakit Umum Universitas Filipina-Filipina (UP-PGH) ditugaskan oleh Menteri Kesehatan Francisco Duque III untuk melakukan analisis independen terhadap catatan 14 anak yang divaksinasi yang meninggal karena berbagai sebab setelah mengikuti program vaksinasi.
Panel tersebut bertugas menemukan bahwa Dengvaxia menyebabkan atau mempengaruhi kematian anak-anak tersebut.
Kejaksaan (PAO) juga melakukan otopsi terhadap anak-anak yang mengikuti program vaksinasi sebelum kematiannya.
Sekelompok dokter, termasuk mantan kepala kesehatan, telah meminta PAO untuk berhenti melakukan otopsi dan membiarkan “ahli patologi forensik yang kompeten” menentukan penyebab kematian anak-anak tersebut.
TONTON sidang DPR hari Senin tentang kontroversi Dengvaxia di sini. – Rappler.com
