Mantan ketua FDA membela surat edaran yang menghapus pengawasan pasca pemasaran
keren989
- 0
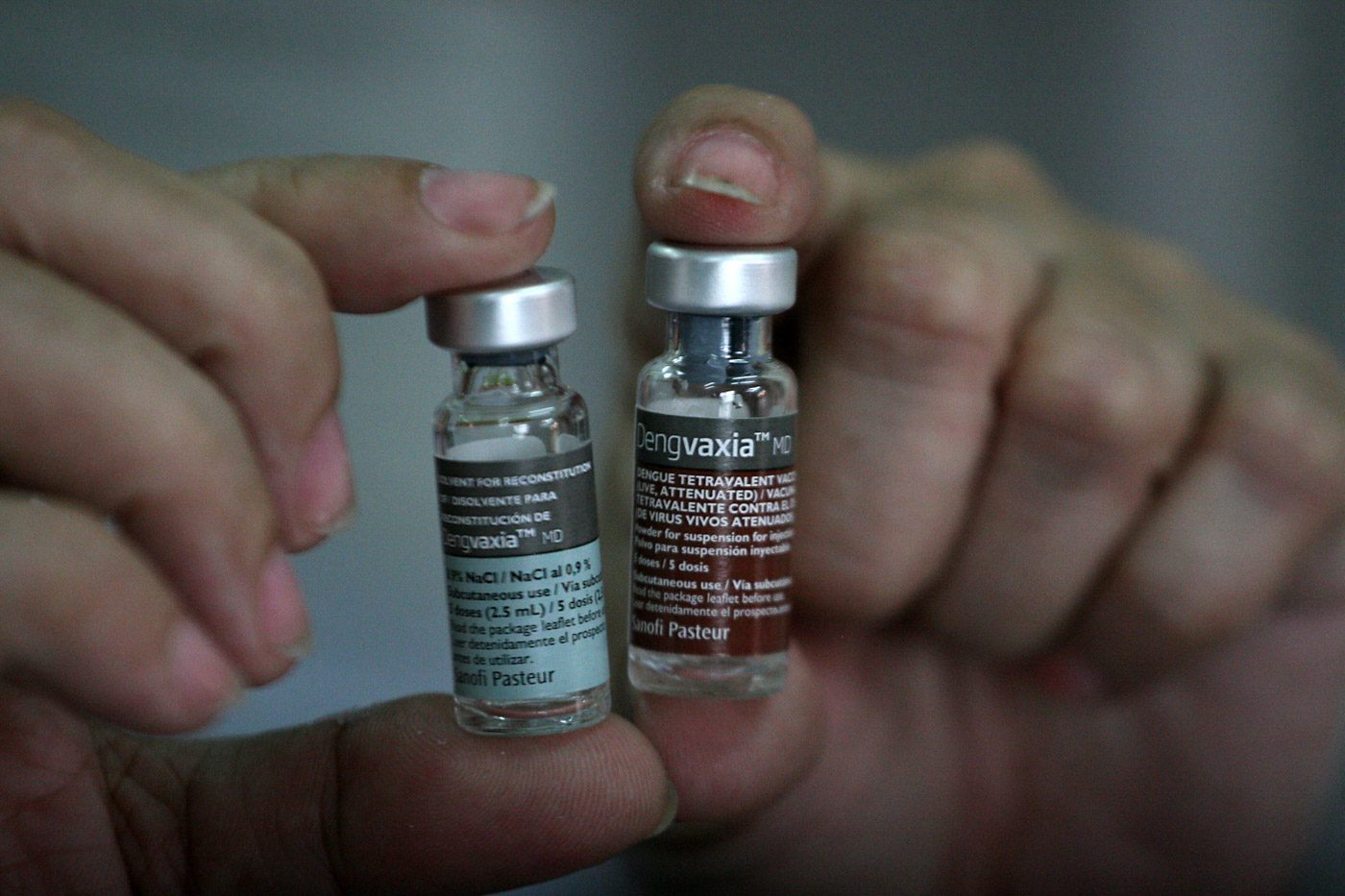
Kenneth Hartigan-Go membela surat edaran yang dikeluarkannya pada tahun 2013 yang mengizinkan vaksin demam berdarah mendapatkan sertifikat registrasi produk (CPR) bahkan tanpa melakukan pengawasan pasca pemasaran.
MANILA, Filipina – Mantan kepala Badan Pengawas Obat dan Makanan (FDA) pada Rabu, 13 Desember, membela surat edaran yang dikeluarkannya pada tahun 2013 yang memperbolehkan vaksin demam berdarah mendapatkan sertifikat registrasi produk (CPR) meski tanpa melakukan pasca- pengawasan pemasaran.
Mantan Direktur Jenderal FDA Kenneth Hartigan-Go disebutkan dalam email oleh seorang saksi yang ditangani oleh Relawan Melawan Kejahatan dan Korupsi. Saksi menyatakan bahwa “dengvaxia mendapat sertifikat registrasi produk super cepat dari FDA di bawah pengawasan Usec Kenneth Hartigan-Go.”
Dalam sidang komite hari Rabu di Dewan Perwakilan Rakyat, Melody Zamudio, pejabat yang bertanggung jawab di Pusat Regulasi dan Penelitian Obat FDA, mengatakan mereka memberikan CPR selama 5 tahun untuk pelepasan Dengvaxia yang dipantau setelah Sanofi fase 1 hingga 3 uji klinis. percobaan.
Mereka tidak memerlukan fase 4 sebelum mengeluarkan CPR karena menurut Zamudio fase 4 merupakan bagian dari pengawasan pasca pemasaran.
“Ada surat edaran yang dikeluarkan oleh Direktur (Jenderal) FDA saat itu Kenneth Hartigan-Go bahwa pasca pemasaran tidak perlu dilakukan di antara masyarakat Filipina. Sebelumnya kami membutuhkan 3.000 pasien dalam pengawasan pelepasan, namun untuk sirkular itu tidak diperlukan lagi. Kami mengambil status global setelah penerbitan CPR sebagai bagian dari pengawasan pasca pemasaran
Perwakilan Distrik 1 Oriental Mindoro Doy Leachon kemudian bertanya kepada Hartigan-Go apakah pertanyaan seputar vaksin demam berdarah akan terjawab jika uji klinis fase 4 saja dilakukan.
“Memo pengawasan pasca pemasaran disiapkan pada tahun 2013 – dua tahun sebelum vaksin demam berdarah. Alasannya adalah untuk memberikan strategi FDA yang lebih kuat dan kokoh dalam proses persetujuan pra-pasar mereka. Kesejahteraan pasienlah yang kami pikirkan ketika kami menyusun surat edaran ini dengan berkonsultasi dengan tim teknis kami dan pemangku kepentingan di industri ini,” jelas Hartigan-Go.
Menurutnya, pengawasan pasca pemasaran sebelum surat edaran tahun 2013 “sangat kurang”.
“Kami telah melihat hal ini disalahgunakan oleh industri dan dokter karena mereka dibayar untuk melakukan ‘studi pemantauan’ dan mereka mengirimkan data yang tidak cukup baik untuk kami deteksi. Karena statistik, 3.000 pasien tidak akan mengalami reaksi merugikan,” dia menambahkan.
(Kami telah melihat industri dan dokter menyalahgunakan hal ini karena mereka dibayar untuk melakukan ‘studi pemantauan’ dan mereka memberikan data yang tidak cukup baik untuk kami deteksi. Berdasarkan hasil statistik, 3.000 pasien, kami tidak mendapatkan hasil yang merugikan. reaksi.)
Hartigan-Go kemudian menyebutkan mekanisme dan strategi lain yang mereka terapkan sebagai pengganti pengawasan pasca-pasar, seperti persyaratan laporan pembaruan keselamatan berkala dan penyerahan rencana manajemen risiko,
“Di luar memo ini, masih ada lagi (ada) strategi lain sesuai dengan Republic Act 9711. Kami telah membentuk unit farmakovigilans yang dapat mengevaluasi semua kasus dari keamanan berkala,” tambahnya.
Namun Dr Tony Leachon, yang menentang penerapan program vaksinasi demam berdarah sejak tahun 2016, mengatakan penghapusan program pengawasan pasca pemasaran “membuka pintu air” bagi obat baru yang mungkin tidak aman.
“Ini tidak merujuk padanya (Kenneth Hartigan-Go), tetapi ketika program pengawasan pasca pemasaran dihapuskan, Anda membuka pintu air bagi obat baru yang mungkin tidak aman untuk dipasarkan, karena pengawasan pasca pemasaran akan melibatkan a hubungan dokter-pasien,” kata Leachon, kakak dari Doy Leachon.
Dr Tony mengatakan hubungan dokter-pasien hilang ketika departemen kesehatan memutuskan untuk melakukan vaksinasi massal. Dia mencatat bahwa hanya ketika suatu produk dianggap aman barulah Dewan Eksekutif Formularium (FEC) bisa diajak berkonsultasi.
“Tetapi dalam masalah khusus ini, bahkan FEC mewajibkan Sanofi dan (Departemen Kesehatan) untuk menyerahkan (pengawasan pasca pemasaran), dan hal itu tidak akan tercapai sebelum vaksinasi massal,” katanya.
Rappler sebelumnya melaporkan bahwa langkah untuk memasukkan vaksin Dengvaxia ke dalam program vaksinasi nasional tidak mendapat izin dari FEC – panel ahli medis yang bertugas meninjau keamanan, efektivitas, dan bahkan efektivitas biaya.
Menteri Kesehatan Francisco Duque III menghentikan program tersebut pada tanggal 1 Desember, sehari setelah raksasa farmasi Perancis Sanofi Pasteur mengungkapkan bahwa Dengvaxia dapat menyebabkan kasus demam berdarah yang lebih parah jika diberikan kepada seseorang yang sebelumnya belum pernah terinfeksi virus tersebut.
Uji coba masih berlangsung hingga postingan ini dibuat. – Rappler.com
